| คุณสมบัติทางเคมี |
ของเหลวไม่มีสี |
| คุณสมบัติทางเคมี |
พิโคลีนเป็นของเหลวไม่มีสี กลิ่นฉุนไม่พึงประสงค์คล้ายไพริดีน "พิโคลีน" มักถูกใช้เป็นไอโซเมอร์ผสม |
| การเกิดขึ้น |
3-เมทิลไพริดีนถูกปล่อยออกมาในระหว่างการผลิตเชื้อเพลิงฟอสซิล มันถูกสร้างขึ้นเป็นผลพลอยได้จากการผลิตโค้ก (Naizer และ Mashek 1974); มีอยู่ในน้ำเสียจากการแปรสภาพเป็นถ่านหิน (Giabbai et al 1985); เป็นสิ่งปนเปื้อนในน้ำใต้ดินใกล้กับแหล่งแปรสภาพเป็นถ่านหินใต้ดิน (Stuermer และ Morris 1982) เป็นส่วนประกอบของน้ำใต้ดินที่ปนเปื้อนด้วยของเสียจากถ่านหิน-น้ำมันดิน (Pereira et al 1983) และพบได้ในน้ำเสียจากชั้นหินน้ำมัน (Hawthorne and Sievers 1984; Hawthorne et al 1985) มันก่อตัวขึ้นจากไพโรไลซิสของไม้ (Yasuhara และ Sugiura 1987) และเป็นส่วนประกอบของบุหรี่ (IARC 1986; Sakuma et al 1984) และควันกัญชา (Merli et al 1981) 3-เมทิลไพริดีนเกิดขึ้นระหว่างการสลายตัวด้วยความร้อนของนิโคตินในการเผาไหม้ยาสูบ (Schmelz et al 1979) สารเคมียังมีอยู่ในกาแฟที่ชงแล้ว (Sasaki et al 1987) และชาดำ (Werkoff และ Hubert 1975) 3-ตรวจพบเมทิลไพริดีนร่วมกับสารมลพิษขนาดเล็กอื่นๆ ในแหล่งน้ำบาร์เซโลนา (Rivera et al 1987) วิธีการบำบัดน้ำเสียทางชีวภาพที่มีสารเคมีสูงได้รับการพัฒนา (Roubiskova 1986) มีการศึกษาความสามารถในการย่อยสลายทางชีวภาพของ 3-เมทิลไพริดีนในดินต่างๆ (Sims and Sommers 1985, 1986) |
| การใช้งาน |
สารตั้งต้นที่มีประโยชน์สำหรับสารเคมีทางการเกษตรและยาแก้พิษสำหรับพิษจากออร์กาโนฟอสเฟต |
| การใช้งาน |
ตัวทำละลาย; ระดับกลางในอุตสาหกรรมสีย้อมและเรซิน ในการผลิตยาฆ่าแมลง สารกันซึม ไนอาซิน และไนอาซินาไมด์ |
| การใช้งาน |
3-พิโคลีนถูกใช้เป็นสารตั้งต้นในอุตสาหกรรมยาและการเกษตร ทำหน้าที่เป็นสารตั้งต้นของ 3-ไซยาโนไพริดีน ไนอาซิน วิตามินบี เป็นยาแก้พิษจากพิษของออร์กาโนฟอสเฟต |
| คำนิยาม |
ChEBI: 3-เมทิลไพริดีนคือเมทิลไพริดีนที่ถูกแทนที่ด้วยไพริดีนด้วยหมู่เมทิลที่ตำแหน่ง 3 |
| วิธีการผลิต |
มีสามวิธีหลักๆ ของ 3-การผลิตเมทิลไพริดีน: (1) ปฏิกิริยาเฟสไอของอะซีตัลดีไฮด์และแอมโมเนียกับฟอร์มาลดีไฮด์และ/หรือเมทานอลต่อหน้าตัวเร่งปฏิกิริยาที่เป็นกรด (เช่น Si02A103); (2) การสกัดจากน้ำมันกระดูก (3) การกลั่นกระดูกหรือถ่านหินแบบแห้ง (Hawley 1977; Parmeggiani 1983) |
| คำอธิบายทั่วไป |
ของเหลวไม่มีสีมีกลิ่นหวาน |
| ปฏิกิริยาอากาศและน้ำ |
ไวไฟสูง. ละลายน้ำได้ |
| โปรไฟล์ปฏิกิริยา |
3-พิโคลีนอาจทำปฏิกิริยากับวัสดุออกซิไดซ์ ทำให้กรดเป็นกลางในปฏิกิริยาคายความร้อนเพื่อสร้างเกลือบวกกับน้ำ อาจเข้ากันไม่ได้กับไอโซไซยาเนต, สารอินทรีย์ที่มีฮาโลเจน, เปอร์ออกไซด์, ฟีนอล (กรด), อีพอกไซด์, แอนไฮไดรด์ และกรดเฮไลด์ ไฮโดรเจนที่เป็นก๊าซไวไฟอาจเกิดขึ้นร่วมกับตัวรีดิวซ์ที่รุนแรง เช่น ไฮไดรด์ |
| อันตรายต่อสุขภาพ |
เป็นอันตรายหากกลืนกิน สูดดม หรือดูดซึมผ่านผิวหนัง สารนี้ทำลายเนื้อเยื่อของเยื่อเมือกและระบบทางเดินหายใจส่วนบน ดวงตา และผิวหนังอย่างรุนแรง การสูดดมอาจถึงแก่ชีวิตได้เนื่องจากอาการกระตุก กล่องเสียงอักเสบและหลอดลมอักเสบ โรคปอดอักเสบจากสารเคมี และอาการบวมน้ำที่ปอด อาการของการสัมผัสอาจรวมถึงอาการแสบร้อน ไอ หายใจมีเสียงหวีด กล่องเสียงอักเสบ หายใจลำบาก ปวดศีรษะ คลื่นไส้และอาเจียน |
| อันตรายต่อสุขภาพ |
อาการทางคลินิกของความเป็นพิษที่เกิดจากอนุพันธ์อัลคิลของไพริดีน รวมทั้งการลดน้ำหนัก ท้องเสีย อ่อนแรง สูญเสียสติ และหมดสติ (RTECS 1988) การเป็นพิษในชายอายุ 32 ปีที่สัมผัสไอระเหยทางอุตสาหกรรมมีลักษณะพิเศษคือการรบกวนของระบบอัตโนมัติที่ไม่ซ้ำใครต่อภูมิหลังที่ไม่สบาย (แองจิโอดีสโทเนีย แนวโน้มไปสู่ภาวะความดันโลหิตต่ำและหัวใจเต้นช้า เพิ่มการสะท้อนกลับของพิโลมอเตอร์ และการรบกวนของการควบคุมอุณหภูมิ) และโดยปรากฏการณ์โพลีนิวริติก (Budanova 1973)
ชายอายุ 58- ปีที่ได้รับ 3-เมทิลไพริดีนจากการประกอบอาชีพเป็นเวลา 11 ปี แสดงให้เห็นว่ามีกลูตามิกไพรูวิกทรานซามิเนสในตับและกลูตามิกออกซาโลอะซิติกทรานซามิเนสเพิ่มขึ้น (Caballeria et al 1979) |
| อันตรายจากไฟไหม้ |
อันตรายพิเศษของผลิตภัณฑ์จากการเผาไหม้: ไอระเหยอาจเดินทางเป็นระยะทางไกลมากไปยังแหล่งกำเนิดประกายไฟและย้อนกลับ ก่อให้เกิดสารผสมที่ระเบิดได้ในอากาศ. ปล่อยควันพิษภายใต้สภาวะที่เกิดเพลิงไหม้ |
| ความไวไฟและการระเบิด |
ไวไฟ |
| ใช้ในอุตสาหกรรม |
{{0}}เมทิลไพริดีนสามารถใช้เป็นตัวทำละลาย สารตัวกลางในอุตสาหกรรมสีย้อมและเรซิน ในการผลิตยาฆ่าแมลง เป็นสารกันซึม ในการสังเคราะห์ยา เป็นสารเร่งปฏิกิริยายางและสารทำปฏิกิริยาในห้องปฏิบัติการ ( ฮอว์ลีย์ 1977; วินด์โฮลซ์ และคณะ 1983) นอกจากนี้ยังใช้เป็นสารเคมีตัวกลางสำหรับการผลิตไนอาซินและไนอาซินาไมด์ (วิตามินต่อต้านเพลลากรา) การผลิตของสหรัฐฯ ในปี 1978 อยู่ที่ประมาณ 1.32-2.07xl07กิโลกรัม (HSDB 1988) |
| โปรไฟล์ความปลอดภัย |
พิษจากทางหลอดเลือดดำและในช่องท้อง เป็นพิษปานกลางเมื่อกลืนกิน. ไวไฟเมื่อสัมผัสกับความร้อนหรือเปลวไฟ สามารถทำปฏิกิริยารุนแรงกับสารออกซิไดซ์ได้ เมื่อถูกความร้อนจนสลายตัวจะปล่อยควันพิษของ NOx |
| สังเคราะห์ |
ในปฏิกิริยาเฟสไอเหนือตัวเร่งปฏิกิริยาที่มีนิกเกิลโดยมีไฮโดรเจน 2-เมทิลกลูตาโรไนไตรล์ให้ 3-เมทิลไพเพอริดีน จากนั้นจึงผ่านการดีไฮโดรจิเนชันเหนือแพลเลเดียม – อลูมินา เพื่อให้ 3-เมทิลไพริดีน:
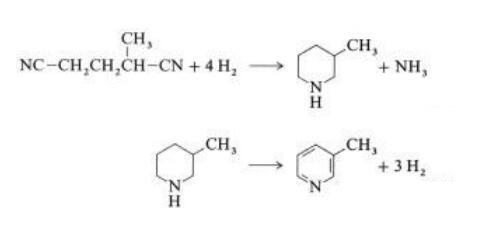
ปฏิกิริยาเฟสก๊าซขั้นตอนเดียวเหนือตัวเร่งปฏิกิริยาที่มีแพลเลเดียมได้รับการรายงานว่าให้ 3-เมทิลไพริดีนในปริมาณ 50 % |
| การรับสัมผัสเชื้อที่เป็นไปได้ |
(โอ-ไอโซเมอร์); สงสัยว่าจะเป็นอันตรายจากพิษต่อระบบสืบพันธุ์, สารระคายเคืองหลัก (ไม่มีปฏิกิริยาภูมิแพ้), (เอ็ม-ไอโซเมอร์): ความเสี่ยงที่เป็นไปได้ในการเกิดเนื้องอก, สารระคายเคืองขั้นต้น (ไม่มีปฏิกิริยาภูมิแพ้) พิโคลีนถูกใช้เป็นตัวกลางในการผลิตยา การผลิตยาฆ่าแมลง และในการผลิตสีย้อมและเคมีภัณฑ์ยาง นอกจากนี้ยังใช้เป็นตัวทำละลาย |
| การก่อมะเร็ง |
ไม่พบการศึกษาที่เชื่อถือได้ในสัตว์เลี้ยงลูกด้วยนมเพื่อประเมินศักยภาพในการก่อมะเร็งของเมทิลไพริดีนทั้งสามชนิด เมทิลไพริดีนไม่มีรายการใดเป็นสารก่อมะเร็งโดย IARC, NTP, OSHA หรือ ACGIH |
| การเผาผลาญอาหาร |
เมทิลไพริดีนสามารถดูดซึมได้โดยการสูดดม การกลืนกิน และการสัมผัสทางผิวหนัง (Parmeggiana 1983) เปอร์เซ็นต์การดูดซึมของ 3-เมทิลไพริดีนโดยหนูเพิ่มขึ้นตามขนาดยา การกำจัดเกิดขึ้นใน 2 ระยะ ระยะเวลาซึ่งขึ้นอยู่กับขนาดยาด้วย (Zharikov และ Titov 1982) การเติมกลุ่มเมทิลลงในไพริดีนช่วยเพิ่มอัตราการดูดซึมเข้าสู่ตับ ไต และสมองของหนูได้อย่างมาก (Zharikov et al 1983) ตำแหน่งของกลุ่มเมทิลมีอิทธิพลอย่างมากต่อเภสัชจลนศาสตร์ของเมทิลไพริดีน โดยที่ 3-เมทิลไพริดีนแสดงครึ่งชีวิตทางชีวภาพที่ยาวที่สุด
การออกซิเดชันของ N เป็นเส้นทางรองสำหรับ 3-การเปลี่ยนรูปทางชีวภาพของเมทิลไพริดีนด้วยการเปลี่ยนรูปทางชีวภาพ 6.6, 4.2 และ 0.7% ของขนาดยา ตามลำดับ โดยถูกขับออกทางปัสสาวะของหนู หนูแรท และหนูตะเภาที่ได้รับ ip ปริมาณสารเคมี (Gorrod และ Damani 1980) การขับถ่ายของ 3-methylpyridine N-ออกไซด์ ในปัสสาวะเพิ่มขึ้นหลังจากการปรับสภาพของหนูด้วยฟีโนบาร์บาร์บิทอล แต่ 3-methylcholanthrene ไม่มีผลกระทบที่เห็นได้ชัดเจนต่อการกำจัด N-ออกไซด์ (Gorrod และ Damani 1979a, 1979b) โครงสร้างของ 3-เมทิลไพริดีน เอ็น-ออกไซด์ได้รับการตรวจสอบโดยแมสสเปกโตรเมทรี (Cowan et al 1978) |
| การส่งสินค้า |
UN2313 พิโคลีน ระดับอันตราย: 3; ป้ายกำกับ: 3-ของเหลวไวไฟ |
| วิธีการทำให้บริสุทธิ์ |
โดยทั่วไป สามารถใช้วิธีการเดียวกันของการทำให้บริสุทธิ์ที่อธิบายไว้สำหรับ 2-เมทิลไพริดีนได้ อย่างไรก็ตาม 3-เมทิลไพริดีนมักประกอบด้วย 4-เมทิลไพริดีนและ 2,6-ลูติดีน ซึ่งทั้งสองอย่างนี้ไม่สามารถกำจัดออกได้อย่างน่าพอใจโดยการทำให้แห้งและการแยกส่วน หรือโดยการใช้สารเชิงซ้อน ZnCl2 Biddiscombe และ Handley [J Chem Soc 1957 1954] หลังจากการกลั่นด้วยไอน้ำสำหรับ 2-เมทิลไพริดีน ให้บำบัดสารตกค้างด้วยยูเรียเพื่อกำจัดลูติดีน 2 6- ตัวออก จากนั้นจึงกลั่นอะซีโอโทรปิคอลด้วยกรดอะซิติก ( อะซีโอโทรปมีค่า b 114.5o/712 มม.) และคืนฐานโดยการเติม NaOH ที่เป็นน้ำ 30% ที่มากเกินไป ทำให้แห้งด้วย NaOH ที่เป็นของแข็งและการกลั่นแบบแยกส่วนอย่างระมัดระวัง จากนั้นการกลั่นจะถูกทำให้ตกผลึกเป็นบางส่วนโดยการแช่แข็งบางส่วนอย่างช้าๆ การรักษาทางเลือก [Reithoff et al. Ind Eng Chem (Anal Edn) 18 458 1946] คือการไหลย้อนฐานน้ำมันดิบ (500 มล.) เป็นเวลา 20-24 ชั่วโมงด้วยส่วนผสมของอะซิติกแอนไฮไดรด์ (125 ก.) และพาทาลิกแอนไฮไดรด์ (125 ก.) ตามด้วยการกลั่นจนเป็นพาทาลิกแอนไฮไดรด์ เริ่มผ่านไป การกลั่นจะได้รับการบำบัดด้วย NaOH (250 กรัมในน้ำ 1.5 ลิตร) จากนั้นจึงกลั่นด้วยไอน้ำ การเติม NaOH ที่เป็นของแข็ง (250 กรัม) ในการกลั่นนี้ (ca 2L) ทำให้เกิดการแยก 3-เมทิลไพริดีน ซึ่งถูกเอาออก ทำให้แห้ง (K2CO3 จากนั้น BaO) และกลั่นแบบแยกส่วน (การแช่แข็งแบบเศษส่วนตามมาอาจจะได้เปรียบ) ไฮโดรคลอไรด์มีค่า m 85o และพิคเรตมีค่า m 153o (จาก Me2CO, EtOH หรือ H2O) [ไบล์สไตน์ 20 III/IV 2710, 20/5 V 506] |
| ความไม่เข้ากัน |
ไอระเหยอาจก่อให้เกิดสารผสมที่ระเบิดได้กับอากาศ. เข้ากันไม่ได้กับออกซิไดเซอร์ (คลอเรต, ไนเตรต, เปอร์ออกไซด์, เปอร์แมงกาเนต, เปอร์คลอเรต, คลอรีน, โบรมีน, ฟลูออรีน ฯลฯ ); การสัมผัสอาจทำให้เกิดเพลิงไหม้หรือการระเบิด เก็บให้ห่างจากวัสดุที่เป็นด่าง, เบสแก่, กรดแก่, ออกโซแอซิด, อีพอกไซด์ โจมตีทองแดงและโลหะผสมของทองแดง |