
การแนะนำสินค้า
| แคลเซียมฟลูออไรด์ ข้อมูลพื้นฐาน |
| สมบัติทางเคมี โครงสร้างผลึก การใช้งาน วิธีการผลิต |
| ชื่อสินค้า : | แคลเซียมฟลูออไรด์ |
| คำพ้องความหมาย : | แคลเซียมฟลูออไรด์;แคลเซียมฟลูออไรด์ 99.9% เป็นโลหะเล็กน้อย;แคลเซียมฟลูออไรด์ 99.95% เป็นโลหะเล็กน้อย;แคลเซียมฟลูออไรด์ ปราศจากน้ำ บรรจุในแอมเพิลภายใต้อาร์กอน 99.99% เป็นโลหะเล็กน้อย;แคลเซียมฟลูออไรด์ในจีน;แอนติบอดี ANTI-CNOT8 (C-TERM) ที่ผลิตในกระต่าย;โปรตีนคล้าย CAF1-;CALIFp |
| CAS: | 7789-75-5 |
| เอ็มเอฟ: | คาฟ2 |
| มว.: | 78.07 |
| เอกสิทธิ์: | 232-188-7 |
| หมวดหมู่สินค้า: | สารอนินทรีย์; โลหะฮาไลด์ |
| ไฟล์โมล: | 7789-75-5.โมล |
 |
|
| คุณสมบัติทางเคมีของแคลเซียมฟลูออไรด์ |
| จุดหลอมเหลว | 1402 องศา |
| จุดเดือด | 2500 องศา (สว่าง) |
| ความหนาแน่น | 3.18 กรัม/มล. ที่ 25 องศา (สว่าง) |
| ดัชนีหักเหแสง | 1.434 |
| เอฟพี | 2500 องศา |
| อุณหภูมิในการจัดเก็บ | -20 องศา |
| ความสามารถในการละลาย | ละลายได้เล็กน้อยในกรด ไม่ละลายในอะซิโตน |
| รูปร่าง | คัน |
| สี | สีขาว |
| ความถ่วงจำเพาะ | 3.18 |
| ความสามารถในการละลายน้ำ | 0.015 กรัมต่อน้ำ 100 กรัมที่อุณหภูมิห้อง (ไม่ละลายน้ำ) |
| อ่อนไหว | ดูดความชื้น |
| เมอร์ค | 14,1667 |
| ค่าคงที่ของผลิตภัณฑ์ความสามารถในการละลาย (Ksp) | พีเคเอสพี: 8.28 |
| ข้อจำกัดในการรับแสง | ACGIH: TWA 2.5 มก./ลบ.ม. NIOSH: IDLH 250 มก./ลบ.ม.; TWA 2.5 มก./ลบ.ม |
| ค่าคงที่ไดอิเล็กตริก | 2.5 (สภาพแวดล้อม) |
| ความเสถียร: | เสถียร แคลเซียมฟลูออไรด์ไม่ทำปฏิกิริยากับสารเคมีอินทรีย์และกรดหลายชนิด รวมถึง HF จะละลายช้าๆ ในกรดไนตริก |
| อินชิคีย์ | วุควิธวัชเซย์-อุฟฟัยซา-แอล |
| การอ้างอิงฐานข้อมูล CAS | 7789-75-5(อ้างอิงฐานข้อมูล CAS) |
| เอกสารอ้างอิงเคมี NIST | แคลเซียมฟลูออไรด์(7789-75-5) |
| ระบบทะเบียนสารของ EPA | แคลเซียมไดฟลูออไรด์ (7789-75-5) |
| ข้อมูลด้านความปลอดภัย |
| รหัสอันตราย | ซีอาน,Xin |
| คำชี้แจงความเสี่ยง | 36/37/38 |
| คำชี้แจงด้านความปลอดภัย | 26-37/39-36 |
| ริดาร | 3288 |
| WGK เยอรมนี | 1 |
| สถาบัน RTECS | EW1760000 |
| หมายเหตุอันตราย | สารระคายเคือง |
| สพฐ. | ใช่ |
| รหัส HS | 28261900 |
| ข้อมูลสารอันตราย | 7789-75-5(ข้อมูลสารอันตราย) |
| ความเป็นพิษ | LD50 ip ในหนู: 2638.27 มก./กก. (Stratmann) |
| ข้อมูล MSDS |
| ผู้ให้บริการ | ภาษา |
|---|---|
| แคลเซียมฟลูออไรด์ | ภาษาอังกฤษ |
| ซิกม่า อัลดริช | ภาษาอังกฤษ |
| อะครอส | ภาษาอังกฤษ |
| อัลฟ่า | ภาษาอังกฤษ |
| การใช้และการสังเคราะห์แคลเซียมฟลูออไรด์ |
| คุณสมบัติทางเคมี | แคลเซียมฟลูออไรด์เป็นส่วนประกอบหลักของฟลูออไรต์หรือฟลูออไรต์ สูตรเคมีคือ CaF2 เป็นผลึกลูกบาศก์ไม่มีสีหรือผงสีขาว ความหนาแน่นสัมพัทธ์คือ 3.18 จุดหลอมเหลวคือ 1423 องศา จุดเดือดอยู่ที่ประมาณ 2500 องศา ความสามารถในการละลายในน้ำน้อยมาก น้ำ 100 กรัมสามารถละลายได้เพียง 0.0016 กรัมที่ 18 องศา ไม่ละลายในอะซิโตน แต่ละลายได้ในกรดไฮโดรคลอริก กรดไฮโดรฟลูออริก กรดซัลฟิวริก กรดไนตริก และสารละลายเกลือแอมโมเนียม และไม่สามารถทำปฏิกิริยากับกรดเจือจางได้ แต่สามารถทำปฏิกิริยากับกรดซัลฟิวริกเข้มข้นร้อนและสร้างกรดไฮโดรฟลูออริกได้ สามารถสร้างสารเชิงซ้อนเมื่อละลายในสารละลายอะลูมิเนียมและเกลือเหล็ก (Fe3 +) แคลเซียมฟลูออไรด์ธรรมชาติเป็นแร่ฟลูออไรต์หรือฟลูออไรด์ มักมีสีเทา เหลือง เขียว ม่วง และสีอื่นๆ บางครั้งก็ไม่มีสี โปร่งใส เป็นกระจกเงา เปราะบาง และมีความหนาแน่นสัมพัทธ์ 3.01~3.25 มีปรากฏการณ์การเรืองแสงที่สำคัญ สามารถใช้เป็นแหล่งกำเนิดฟลูออรีนและเป็นวัสดุในการทำระบบกรดไฮโดรฟลูออริก ฟลูออไรด์ และยังใช้ในการผลิตแก้ว เคลือบฟัน ฟลูออไรด์ส่วนใหญ่ใช้เป็นฟลักซ์ในโลหะวิทยา ฟลูออไรด์บริสุทธิ์มากสามารถใช้ทำเลนส์พิเศษได้ น้ำที่มีแคลเซียมฟลูออไรด์ (1~1.5) × 10-6 สามารถป้องกันปัญหาทางทันตกรรมได้ นอกจากนี้ยังสามารถใช้ในการถลุงเหล็กและเหล็กกล้า สารเคมี แก้ว การผลิตเซรามิก ผลิตภัณฑ์บริสุทธิ์สามารถใช้เป็นตัวเร่งปฏิกิริยาการคายน้ำ การคายไฮโดรเจน โดยผลของเกลือแคลเซียมที่ละลายน้ำได้ (แคลเซียมคาร์บอเนต หรือ แคลเซียมไฮดรอกไซด์) และโซเดียมฟลูออไรด์ หรือกรดไฮโดรฟลูออริก สามารถรับแอมโมเนียมฟลูออไรด์ แคลเซียมฟลูออไรด์ได้ |
| โครงสร้างผลึก | แคลเซียมฟลูออไรด์เป็นผลึกไอออนิกที่มีไอออนฟลูออรีนอยู่ในกลุ่มลูกบาศก์อย่างง่าย และมีไอออนแคลเซียมในครึ่งหนึ่งของไซต์ลูกบาศก์ของโครงสร้าง ไอออนแคลเซียมอาจคิดได้ว่าอยู่บนโครงตาข่าย fcc ที่ "ขยาย" โดยที่ไอออนฟลูออรีนทำให้โครงตาข่ายแยกจากกันที่ 0.39 นาโนเมตร การแสดงนี้แสดงไว้ในแผนภาพด้านล่าง เซลล์ยูนิตมี Ca 42+ไอออนและ 8 F1-ไอออน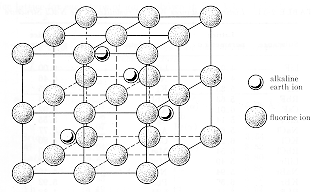 วัสดุนี้โปร่งใสในช่วงสเปกตรัมที่มองเห็นได้ และแสดงการดูดซับแสงอิเล็กทรอนิกส์ในรังสีอัลตราไวโอเลต และการดูดซับแสงของโครงตาข่ายในอินฟราเรด |
| การใช้งาน |
อุตสาหกรรม
แอปพลิเคชัน
บทบาท/ประโยชน์
การผลิตสารเคมี
การผลิตกรดไฮโดรฟลูออริกและฟลูออไรด์
วัตถุดิบ/แหล่งของฟลูออไรด์
การผลิตสารเคมีฟลูออรีนละเอียดและคริโอไลต์สังเคราะห์
วัตถุดิบ/แหล่งของฟลูออไรด์
วัสดุทางสถาปัตยกรรม
การผลิตกระจก
สารช่วยฟลักซ์/ส่งเสริมการหลอมละลายของวัตถุดิบ
การผลิตปูนซีเมนต์
สารช่วยสร้างแร่ธาตุ
การผลิตเคลือบเซรามิก
ฟลักซ์และตัวช่วยระบายสี
โลหะวิทยา
การถลุงเหล็กและเหล็กกล้า การผลิตเฟอร์โรอัลลอยด์ ฯลฯ
สารช่วยฟลักซ์/ลดจุดหลอมเหลวของสารทนไฟ
ยา
การรักษา ควบคุม ป้องกัน และบรรเทาอาการภูมิแพ้
ส่งเสริมการสร้างกระดูกใหม่
ระบบถ่ายภาพความร้อน สเปกโตรสโคปี กล้องโทรทรรศน์ และเลเซอร์เอ็กไซเมอร์
การผลิตส่วนประกอบออปติก เช่น หน้าต่างและเลนส์
วัตถุดิบ/ช่วงความถี่แสงส่งผ่านที่กว้าง ดัชนีหักเหแสงต่ำ เสถียรภาพทางความร้อนสูง
คนอื่น
การผลิตสารเชื่อม
ส่วนประกอบที่สำคัญในสารเคลือบลวดเชื่อมและผงเชื่อม
ปฏิกิริยาการคายน้ำและการกำจัดไฮโดรเจน
ตัวเร่งปฏิกิริยา/เร่งกระบวนการเกิดปฏิกิริยา
การผลิตผ้าเบรค
สารเติมแต่ง/ช่วยลดการเสียดสีที่เกิดจากความร้อนสูงและแรงเสียดทาน
|
| วิธีการผลิต | แหล่งแร่ฟลูออไรต์ที่พบในจีนนั้นส่วนใหญ่ใช้ในการทำเหมืองโดยใช้วิธีการขุดใต้ดิน หรือการทำเหมืองแบบเปิดหน้าดินตื้น และการทำเหมืองใต้ดินแบบลึก สำหรับแร่ที่มีเส้นแร่เอียงมากที่สุด การขยายออกก็ใหญ่เช่นกัน วิธีการทำเหมืองนั้นใช้วิธีการหดตัวในหลุมตื้น กระบวนการทำเหมืองนั้นใช้ "หินฟอสเฟต" วิธีการแยกแร่โดยทั่วไปมี 2 ประเภท ประเภทหนึ่งคือแร่ดิบที่สามารถกลายเป็นแร่เข้มข้นที่มีคุณสมบัติผ่านเกณฑ์ได้โดยการจัดการที่คัดเลือกมา ประเภทที่สองคือแร่และกากแร่ที่คัดเลือกด้วยมือ |
| คำอธิบาย | แคลเซียมฟลูออไรด์เป็นสารผลึกหรือผงสีขาวไม่มีสี มวลโมเลกุล{{0}}.08; ความถ่วงจำเพาะ (H2O:1)=3.18 ที่ 20 องศา; จุดเดือด=2495 องศา; จุดเยือกแข็ง/จุดหลอมเหลว=1423 องศา การระบุอันตราย (ตามระบบการจัดอันดับ NFPA-704 M): สุขภาพ 2, ความไวไฟ 0, ปฏิกิริยา 0 แทบไม่ละลายในน้ำ |
| คุณสมบัติทางเคมี | แคลเซียมฟลูออไรด์ (CaF2) หรือที่เรียกอีกอย่างว่าฟลูออไรต์และเฟลด์สปาร์ เป็นของแข็งไม่มีสีที่ประกอบด้วยผลึกลูกบาศก์ มีความสามารถในการละลายน้ำต่ำ แต่ละลายได้ง่ายในสารละลายเกลือแอมโมเนียม แคลเซียมฟลูออไรด์ใช้ในการสังเคราะห์กรดไฮโดรฟลูออริกและในกระจกกัดกร่อน แคลเซียมฟลูออไรด์ไม่ดูดความชื้นและค่อนข้างเฉื่อย มีความทนทานต่อความร้อนและแรงกระแทกทางกลสูงเพียงพอ และสามารถนำไปผลิตเป็นเครื่องตรวจจับรูปทรงต่างๆ ได้อย่างง่ายดาย แคลเซียมฟลูออไรด์มีแรงดันไอต่ำมาก จึงสามารถใช้ในแอปพลิเคชันสุญญากาศที่หลากหลายได้ ไม่ละลายน้ำและตัวทำละลายอินทรีย์ส่วนใหญ่ ทำให้สามารถนำตัวอย่างกัมมันตภาพรังสีในสารละลายมาสัมผัสกับผลึกได้โดยตรง แคลเซียมฟลูออไรด์เป็นวัสดุโปร่งใสที่ใช้สำหรับตรวจจับรังสี - สูงถึงหลายร้อย keV และสำหรับตรวจจับอนุภาคที่มีประจุ เนื่องจากมีเลขอะตอมต่ำ โฟโตแฟรกชันของวัสดุจึงค่อนข้างเล็ก ซึ่งจำกัดการใช้งานในสเปกโตรมิเตอร์รังสี - ที่พลังงานสูงกว่า อย่างไรก็ตาม เลขอะตอมต่ำทำให้แคลเซียมฟลูออไรด์เป็นวัสดุที่เหมาะสำหรับการตรวจจับอนุภาค - เนื่องจากมีการกระเจิงกลับในปริมาณเล็กน้อย |
| คุณสมบัติทางกายภาพ | ผลึกหรือผงลูกบาศก์สีขาว ดัชนีหักเหแสง 1.434 ความหนาแน่น 3.18 g/cm3 ความแข็ง 4 โมห์ส หลอมเหลวที่ 1,418 องศา ระเหยที่อุณหภูมิ 2,533 องศา ไม่ละลายในน้ำ (16 มก./ล. ที่ 20 องศา) Ksp 3.9x10-11 ละลายได้เล็กน้อยในกรดแร่เจือจาง ละลายได้ในกรดเข้มข้น (เมื่อทำปฏิกิริยา) |
| การใช้งาน | CaF2 ที่เกิดขึ้นตามธรรมชาติเป็นแหล่งหลักของไฮโดรเจนฟลูออไรด์ ซึ่งเป็นสารเคมีที่ใช้ในการผลิตวัตถุดิบต่างๆ มากมาย ฟลูออไรด์จะถูกปลดปล่อยออกมาจากแร่ธาตุโดยการกระทำของกรดซัลฟิวริกเข้มข้น: CaF2 (ของแข็ง)+H2SO4 (ของเหลว)→CaSO4 (ของแข็ง)+2HF (ก๊าซ) CaF2 ถูกใช้เป็นส่วนประกอบทางแสงเนื่องจากมีความเสถียรทางเคมีภายใต้สภาวะที่ไม่เอื้ออำนวย แคลเซียมฟลูออไรด์มักใช้เป็นวัสดุหน้าต่างสำหรับความยาวคลื่นอินฟราเรดและอัลตราไวโอเลต เนื่องจากมีความโปร่งแสงในบริเวณเหล่านี้ (ประมาณ 0.15 ถึง 9 มม.) และมีดัชนีการหักเหของแสงที่ต่ำมาก แคลเซียมฟลูออไรด์เป็นแหล่งแคลเซียมที่ไม่ละลายน้ำสำหรับใช้ในงานที่ไวต่อออกซิเจน เช่น การผลิตโลหะ สารประกอบฟลูออไรด์มีความเข้มข้นต่ำมาก (ppm) สำหรับการใช้งานด้านสุขภาพ สารประกอบฟลูออไรด์ยังมีการใช้งานที่สำคัญในเคมีอินทรีย์สังเคราะห์อีกด้วย นอกจากนี้ยังมักใช้กับโลหะผสมและการสะสมด้วยแสง นอกจากนี้ยังใช้เป็นฟลักซ์ในการหลอมและแปรรูปเหล็ก เหล็กกล้า และวัสดุผสมด้วยของเหลว การทำงานของฟลักซ์ขึ้นอยู่กับจุดหลอมเหลวที่ใกล้เคียงกับเหล็ก ความสามารถในการละลายออกไซด์ และความสามารถในการทำให้ออกไซด์และโลหะเปียก |
| การใช้งาน | ฟลูออไรด์เป็นแหล่งกำเนิดฟลูออรีนและสารประกอบหลัก ในโลหะวิทยาเหล็ก ฟลูออไรด์ถูกใช้เป็นฟลักซ์เพื่อเพิ่มความลื่นไหลของตะกรัน อุตสาหกรรมเหล็กเป็นผู้บริโภครายใหญ่ที่สุด รองลงมาคืออุตสาหกรรมเคมี และอันดับสามคืออุตสาหกรรมแก้วและเซรามิก ฟลูออไรด์สังเคราะห์ใช้ในอุตสาหกรรมออปติก (ส่งผ่านรังสี UV) และแคลเซียมฟลูออไรด์บริสุทธิ์ใช้เป็นตัวเร่งปฏิกิริยาในการคายน้ำและการกำจัดไฮโดรเจน ใช้ในการเติมฟลูออไรด์ในน้ำดื่ม |
| การใช้งาน | แคลเซียมฟลูออไรด์เป็นแหล่งสำคัญของสารประกอบฟลูออไรด์ในเชิงพาณิชย์ เช่นเดียวกับไฮโดรเจนฟลูออไรด์ แคลเซียมฟลูออไรด์มีความโปร่งใสตั้งแต่ช่วงอัลตราไวโอเลตจนถึงอินฟราเรด แคลเซียมฟลูออไรด์ใช้ในระบบสเปกโตรสโคปี ระบบถ่ายภาพความร้อน และเลเซอร์เอกไซเมอร์ นอกจากนี้ยังใช้ในการผลิตส่วนประกอบออปติก เช่น หน้าต่าง ปริซึม และเลนส์ นอกจากนี้ แคลเซียมฟลูออไรด์ยังใช้ในอุตสาหกรรมโลหะวิทยาอะลูมิเนียม การผลิตผ้าเบรก และเคลือบฟันอีกด้วย |
| คำนิยาม | แคลเซียมฟลูออไรด์รูปแบบบริสุทธิ์จากธรรมชาติ |
| วิธีการผลิต | ผลิตภัณฑ์เชิงพาณิชย์ได้มาจากแร่ฟลูออไรด์ที่เกิดขึ้นตามธรรมชาติ ซึ่งผ่านกระบวนการทำให้บริสุทธิ์และบดเป็นผง นอกจากนี้ ยังอาจตกตะกอนได้โดยการผสมสารละลายโซเดียมฟลูออไรด์กับเกลือแคลเซียมที่ละลายน้ำได้: คา(ไม่3)2+ 2NaF → CaF2+ นาโน3 อีกวิธีหนึ่งอาจได้รับโดยการบำบัดแคลเซียมคาร์บอเนตด้วยกรดไฮโดรฟลูออริก:CaCO3+ 2HF → CaF2+ ซีโอ2 + H2O. |
| คำนิยาม | รูปแบบแร่ธาตุของแคลเซียมฟลูออไรด์ (CaF2)ใช้ในการผลิตซีเมนต์และแก้วบางชนิด |
| คำอธิบายทั่วไป | ผงหรือเม็ดสีเทาไม่มีกลิ่น จมน้ำ |
| โปรไฟล์ปฏิกิริยา | แคลเซียมฟลูออไรด์มีกำลังออกซิไดซ์หรือรีดิวซ์ต่ำ อย่างไรก็ตาม ปฏิกิริยารีดอกซ์ยังคงเกิดขึ้นได้ สารประกอบส่วนใหญ่ในกลุ่มนี้ละลายน้ำได้เล็กน้อยหรือไม่ละลายน้ำ หากละลายน้ำได้ แสดงว่าสารละลายไม่มีฤทธิ์เป็นกรดหรือเบสรุนแรง สารประกอบเหล่านี้ไม่ทำปฏิกิริยากับน้ำ |
| อันตราย | สารระคายเคือง |
| อันตรายต่อสุขภาพ | ความเป็นพิษเฉียบพลันเล็กน้อย |
| ความไวไฟและการระเบิดได้ | ไม่ติดไฟ |
| การใช้ในอุตสาหกรรม | ฟลูออไรต์ หรือ ฟลูออสปาร์ เป็นแร่ผลึกหรือเม็ดขนาดใหญ่ที่มีองค์ประกอบ CaF2ใช้เป็นฟลักซ์ในการผลิตเหล็ก สำหรับการผลิตกรดไฮโดรฟลูออริก ในแก้วโอปอล ในเคลือบเซรามิก สำหรับการขูดไครโอไลต์เทียม เป็นสารยึดเกาะสำหรับล้อขัดแก้ว และในการผลิตปูนซีเมนต์ขาว เป็นฟลักซ์ที่ดีกว่าหินปูนสำหรับเหล็ก ทำให้เป็นตะกรันเหลว และปลดปล่อยกำมะถันและฟอสฟอรัสออกจากเหล็ก กรดสปาร์เป็นเกรดที่ใช้ในการผลิตกรดไฮโดรฟลูออริก นอกจากนี้ยังใช้ในการผลิตสารทำความเย็น พลาสติก และสารเคมี และสำหรับการลดปริมาณอะลูมิเนียม ฟลูออไรด์ออปติคัลเป็นเกรดสูงสุดแต่ไม่เป็นที่นิยม ผลึกฟลูออไรด์สำหรับเลนส์ออปติคัลปลูกขึ้นโดยเทียมจากฟลูออไรด์เกรดกรด แคลเซียมฟลูออไรด์บริสุทธิ์ Ca2F6เป็นผงผลึกไม่มีสีที่ใช้สำหรับกัดกระจก ในเคลือบ และเพื่อลดแรงเสียดทานในตลับลูกปืนเครื่องจักร นอกจากนี้ยังใช้สำหรับชิ้นส่วนเซรามิกที่ทนต่อกรดไฮโดรฟลูออริกและกรดอื่นๆ ส่วนใหญ่ แคลเซียมฟลูออไรต์มีซิลิกอนในโมเลกุลและเป็นผงผลึกที่ใช้สำหรับเคลือบ ผลึกฟลูออไรด์รอมบิกใสที่ใช้สำหรับแปลงพลังงานไฟฟ้าเป็นแสง ได้แก่ ตะกั่วฟลูออไรด์ PbF2. |
| โปรไฟล์ความปลอดภัย | เป็นพิษปานกลางเมื่อเข้าสู่ช่องท้อง เป็นพิษเล็กน้อยเมื่อกลืนกิน สารก่อพิษต่อทารกในครรภ์ที่ทดลองแล้ว ผลกระทบต่อระบบสืบพันธุ์อื่นๆ ที่ทดลองแล้ว มีการรายงานข้อมูลการกลายพันธุ์ ดูฟลูออไรด์และสารประกอบแคลเซียมด้วย เมื่อถูกความร้อนจนสลายตัว จะปล่อยไอพิษของ F- |
| การรับสัมผัสเชื้อที่เป็นไปได้ | แคลเซียมฟลูออไรด์ใช้ในการผลิตกรดไฮโดรฟลูออริก เป็นฟลักซ์ในการผลิตเหล็ก ในการถลุง การเชื่อมด้วยไฟฟ้า การทำแก้วและเซรามิก และในการเติมฟลูออไรด์ในน้ำดื่ม |
| ปฐมพยาบาล | หากสารเคมีเข้าตา ให้ถอดคอนแทคเลนส์ออกทันทีและล้างตาทันทีเป็นเวลาอย่างน้อย 15 นาที โดยเปิดเปลือกตาทั้งบนและล่างเป็นครั้งคราว ไปพบแพทย์ทันที หากสารเคมีสัมผัสผิวหนัง ให้ถอดเสื้อผ้าที่ปนเปื้อนออกแล้วล้างด้วยสบู่และน้ำทันที ไปพบแพทย์ทันที หากสูดดมสารเคมีนี้เข้าไป ให้ถอดออกจากที่สัมผัส เริ่มการช่วยหายใจ (โดยใช้มาตรการสากล รวมทั้งสวมหน้ากากช่วยหายใจ) หากหยุดหายใจ และทำ CPR หากหัวใจหยุดเต้น ให้รีบนำส่งสถานพยาบาลทันที เมื่อกลืนสารเคมีนี้เข้าไป ให้ไปพบแพทย์ แพทย์หรือเจ้าหน้าที่พยาบาลที่ได้รับอนุญาตอาจพิจารณาใช้เจลอะลูมิเนียมไฮดรอกไซด์ หากยังมีสติอยู่ |
| พื้นที่จัดเก็บ | รหัสสี-เขียว: สามารถจัดเก็บทั่วไปได้ เก็บในภาชนะที่ปิดสนิทในบริเวณที่เย็นและมีอากาศถ่ายเทได้ดี ห่างจากกรดและโลหะที่มีฤทธิ์ทางเคมี (เช่น โพแทสเซียม โซเดียม แมกนีเซียม และสังกะสี) เนื่องจากจะผลิตไฮโดรเจนฟลูออไรด์ที่กัดกร่อน |
| การส่งสินค้า | แคลเซียมฟลูออไรด์ไม่ได้รับการครอบคลุมโดยเฉพาะโดย DOT ในมาตรฐานบรรจุภัณฑ์ที่เน้นประสิทธิภาพ |
| ความไม่เข้ากัน | ฝุ่นละอองอาจรวมตัวกันเป็นส่วนผสมที่ระเบิดได้กับอากาศ ทำปฏิกิริยากับน้ำ อากาศชื้น และไอน้ำ ปล่อยก๊าซไฮโดรเจนที่ติดไฟได้ และอาจติดไฟเองในอากาศ ตัวรีดิวซ์ที่แรง เข้ากันไม่ได้กับสารออกซิไดเซอร์ (คลอเรต ไนเตรต เปอร์ออกไซด์ เปอร์แมงกาเนต เปอร์คลอเรต คลอรีน โบรมีน ฟลูออรีน เป็นต้น) การสัมผัสอาจทำให้เกิดไฟไหม้หรือระเบิดได้ เก็บให้ห่างจากวัสดุที่มีฤทธิ์เป็นด่าง เบสแรง กรดแรง ออกโซแอซิด อีพอกไซด์ เข้ากันไม่ได้กับฮาโลเจนเนตของโลหะ ซิลเวอร์ฟลูออไรด์ และเทตระไฮโดรฟิวแรน |
| ผลิตภัณฑ์และวัตถุดิบสำหรับการเตรียมแคลเซียมฟลูออไรด์ |
| วัตถุดิบ | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->แคลเซียมแมกนีเซียมฟอสเฟต (CMP) |
| ผลิตภัณฑ์เตรียมอาหาร | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->แมกนีเซียมเฮกซะฟลูออโรอะเซทิลอะเซโทเนตไดไฮเดรต |
ป้ายกำกับยอดนิยม: สังกะสีฟลูออไรด์ ผู้ผลิต ซัพพลายเออร์ โรงงาน สังกะสีฟลูออไรด์ของจีน
คู่ของ: เซอร์โคเนียมฟลูออไรด์
ถัดไป: แคลเซียมฟลูออไรด์
คุณอาจชอบ
ส่งคำถาม


